A Universidade de Oxford e a AstraZeneca se tornaram na terça-feira os primeiros fabricantes de vacinas COVID-19 a publicar dados de testes clínicos em estágio final em um jornal científico, eliminando um obstáculo importante na corrida global para produzir medicamentos seguros e eficazes para o coronavírus.
O estudo, publicado na respeitada revista médica Lancet, confirmou que a vacina funciona em uma média de 70 por cento dos casos.
Ele surge durante uma onda de desenvolvimentos positivos que aumentaram a esperança de que o lançamento de vacinas possa ajudar a conter uma pandemia que matou mais de 1,5 milhão de pessoas e atingiu sociedades em todo o mundo.
A Grã-Bretanha se tornou na terça-feira o primeiro país do mundo ocidental a iniciar a imunização, usando uma vacina rival desenvolvida pela Pfizer-BioNTech depois de aprová-la para uso geral na semana passada.
Os pioneiros Pfizer-BioNTech e a empresa de biotecnologia dos Estados Unidos Moderna relataram eficácia de 95% e 94%, respectivamente, e forneceram dados aos reguladores.
Mas a AstraZeneca é a primeira a ter seus resultados de eficácia de teste confirmados em um artigo científico, disse o Lancet.
Andrew Pollard, o diretor do Oxford Vaccine Group que liderou o estudo, disse que a publicação mostrou que os desenvolvedores estavam compartilhando dados de forma “transparente”, acrescentando que uma variedade de vacinas seria necessária.
“Isso realmente não pode ser uma competição entre desenvolvedores, tem que ser uma competição contra o vírus”, disse ele em uma coletiva de imprensa.
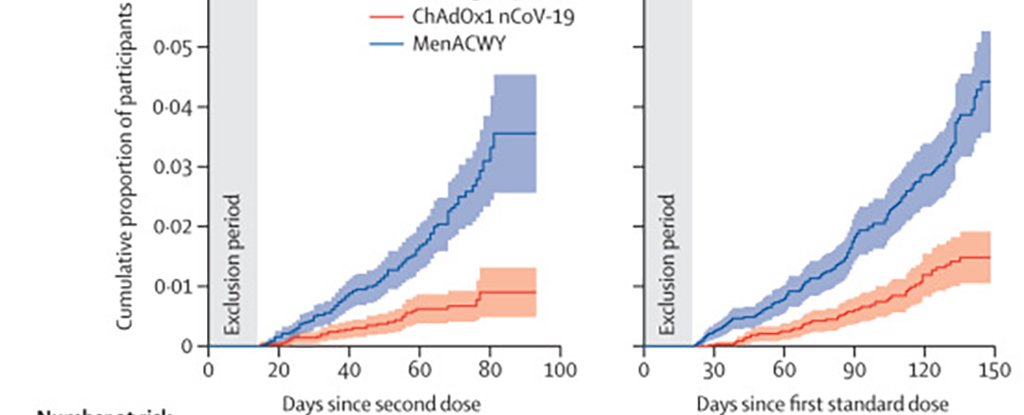
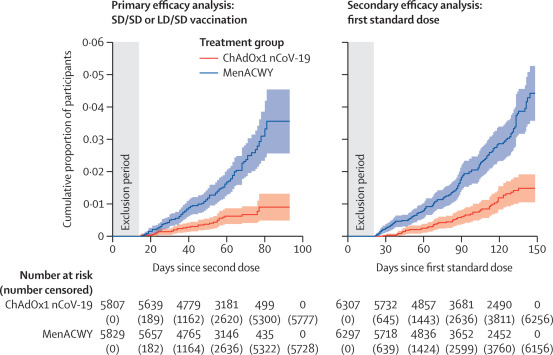
O estudo mostrou que a vacina tinha uma eficácia de 62 por cento para aqueles que receberam duas doses completas, e de 90 por cento para aqueles que receberam meia dose e depois uma dose completa.
A AstraZeneca e Oxford enfrentaram dúvidas sobre seus resultados quando divulgaram uma visão geral no mês passado, depois que descobriram que a meia dose foi administrada por causa de um erro.
Houve também a preocupação de que este grupo de meia dose – 1.367 participantes – não incluísse adultos com mais de 55 anos.
Os pesquisadores disseram que forneceram uma análise extra aos revisores do Lancet, sugerindo que os melhores resultados para o grupo de meia dose não se deviam a outros fatores, como a idade.
Pollard disse que uma vez que os pesquisadores perceberam a discrepância de medição, ela foi incorporada ao ensaio com a concordância dos reguladores.
“Acho que é justo dizer que é preciso investigar mais para explicar o resultado intrigante”, disse ele.
A AstraZeneca disse que caberia aos reguladores decidir as recomendações de dosagem com base nos dados fornecidos.
‘Dilema’
Os resultados são susceptíveis de apresentar um “dilema” para as autoridades farmacêuticas, disse Simon Clarke, Professor Associado de Microbiologia Celular da Universidade de Reading.
Ele disse que enquanto o regime de meia dose mostrou melhor proteção contra doenças e também na redução da transmissão assintomática, o grupo era “relativamente pequeno” e não continha idosos.
“Ainda é possível que se os reguladores permitissem que a vacina fosse usada dessa maneira, o grupo de maior risco não estaria protegido”, disse ele.
Para calcular a eficácia, os autores analisaram os dados da fase 3 – estágio final – ensaios clínicos na Grã-Bretanha e no Brasil, envolvendo 11.636 pessoas, metade das quais recebeu a vacina de qualquer dosagem e a outra metade um placebo.
Eles encontraram 131 casos de COVID-19 sintomático mais de 14 dias após a segunda dose da vacina – 30 no grupo da vacina e 101 no grupo de controle, ou uma eficácia média de 70 por cento.
O estudo disse que não houve hospitalizações ou doenças graves relatadas no grupo da vacina COVID-19 até agora.
Os pesquisadores disseram que a vacina era “segura” após analisar dados de um total de 23.745 participantes em testes na Grã-Bretanha, Brasil e África do Sul.
Um participante do grupo da vacina desenvolveu mielite transversa – um distúrbio neurológico – que estava “possivelmente” relacionado à droga.
Mas eles se recuperaram e continuam a fazer parte do teste, disse o estudo.
A AstraZeneca disse em um comunicado que começou a fornecer dados para reguladores em todo o mundo e está buscando autorização para uso emergencial da Organização Mundial da Saúde para acelerar a disponibilidade potencial em países de baixa renda.
Se aprovado, tem como objetivo produzir até três bilhões de doses em 2021.
Publicado em 10/12/2020 11h14
Artigo original:
Estudo original:


