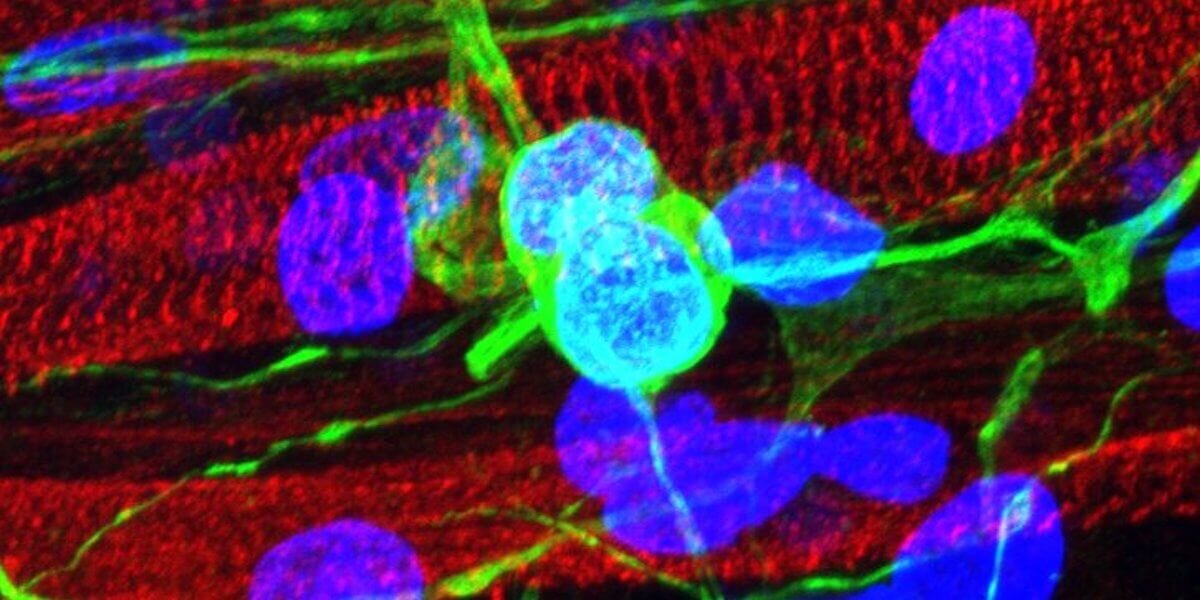
Na luta contra doenças como ALS [Esclerose lateral amiotrófica], pesquisadores de engenharia biomédica do USC Viterbi criaram um modelo de laboratório poderoso para ver melhor como nossos músculos e neurônios se conectam.
As doenças neuromusculares são debilitantes e principalmente incuráveis, afetando 160 em cada 100.000 pessoas em todo o mundo. Distúrbios como ELA e esclerose múltipla afetam a função dos músculos, causando desgaste muscular e perda da função motora. Um grande obstáculo na luta contra essas doenças é o fato de ser notoriamente difícil cultivar tecidos em um laboratório que mostre a conexão entre nossos músculos e os neurônios que os controlam. Até agora.
Ph.D. em engenharia biomédica alunos da Escola de Engenharia USC Viterbi criaram um novo modelo de tecido desenvolvido em laboratório amplamente aprimorado que oferece uma visão mais estável da junção neuromuscular – uma parte importante do nosso sistema que traduz os impulsos elétricos gerados pelos neurônios em nossa coluna em atividade elétrica e movimento em nossas fibras musculares.
A pesquisa foi publicada na APL Bioengineering e foi liderada por Jeffrey Santoso, um Ph.D. estudante no Laboratório de Engenharia de Sistemas Vivos, liderado pela Professora Associada Megan McCain, a Cadeira de Início de Carreira da Chonette.
Santoso disse que a junção neuromuscular é uma conexão altamente estruturada, com dobras em forma de pretzel que aumentam a área de comunicação entre um neurônio e um músculo.
“A junção neuromuscular é o espaço onde o neurônio vai liberar moléculas sinalizadoras chamadas neurotransmissores, que então se ligam a receptores localizados na superfície das fibras musculares”, disse Santoso. “E quando essas moléculas se ligam a esses receptores, isso faz com que a célula muscular seja despolarizada – então há uma mudança de voltagem – e é isso que faz com que seus músculos se contraiam.”
Nas doenças neuromusculares – bem como no processo natural de envelhecimento – muitas vezes há estresse, ou uma quebra na conexão, dentro da junção neuromuscular. Ter modelos precisos de tecido cultivado em laboratório é crucial para entender a degeneração relacionada à idade ou a progressão da doença neuromuscular, bem como os tratamentos mais eficazes. No entanto, os pesquisadores têm lutado para replicar essa conexão complexa, ou ponto de inervação, em modelos de laboratório quando tentam fazer crescer fibras musculares e neurônios juntos.
“Tradicionalmente, quando músculos e neurônios são cultivados juntos em um prato, a estrutura esperada no ponto de inervação está ausente”, disse Santoso, “levando a um tecido funcionalmente inepto que não representa a fisiologia adequada, tornando difícil tirar conclusões sobre doenças e drogas potenciais. ”
Como resultado, os modelos de tecido anteriores tendem a morrer após duas semanas. Para criar um modelo de laboratório mais útil, Santoso e seus co-autores desenvolveram uma plataforma de gel à base de gelatina que permite que um músculo esquelético cresça no laboratório em sua arquitetura alinhada adequada, mantendo sua estrutura por pelo menos um mês e gerando contrações semelhante à força do tecido humano nativo.
“Quando você tenta cultivar o tecido em laboratório, geralmente envolve o crescimento de células musculares em uma camada e a colocação das células neuronais no topo”, disse Santoso. “A junção que se forma não cria uma estrutura dessas dobras parecidas com pretzel, e isso causa uma variedade de problemas, porque pode não responder a certas drogas como você esperaria.”
Quando Santoso e sua equipe combinaram seu músculo esquelético desenvolvido em laboratório com neurônios motores derivados de células-tronco em sua plataforma de gelatina, eles descobriram que o músculo formou junções neuromusculares mais estruturadas com sucesso.
Santoso disse que os modelos de tecido anteriores costumavam usar pratos rígidos de plástico ou vidro que não ofereciam o tipo certo de ambiente de proteína para o tecido e muitas vezes faziam com que as células musculares se desprendessem quando contraídas, resultando na morte das células.

“O hidrogel de gelatina que estamos usando, como um biomaterial natural, é naturalmente adesivo às células do músculo esquelético, e esse é um dos motivos pelos quais pudemos ver nosso modelo de tecido amadurecendo muito mais do que muitos outros modelos anteriores”, disse Santoso disse. “O músculo esquelético pode sobreviver na superfície por um período mais longo de tempo, e ter esse tempo maior na cultura significa que, quando introduzimos os neurônios motores na cultura, ele pode se integrar totalmente para criar essa junção neuromuscular.”
Santoso disse que estudar as doenças neuromusculares foi especialmente desafiador, porque o sistema neuromuscular humano é muito complexo. Os neurônios motores residem em nossa medula espinhal e devem passar por um elaborado caminho de conexões para alcançar todos os músculos de nosso corpo.
“Existem tantos lugares neste caminho onde as coisas podem dar errado”, disse Santoso. “Por causa disso, você precisa que o modelo de laboratório seja bem próximo em função e estrutura, em comparação com o que você vê nos seres vivos.”
A equipe de pesquisa agora está procurando expandir seus colaboradores de pesquisa para que possam aplicar sua plataforma de modelo de tecido a células derivadas de pacientes humanos.
“No momento, as doenças neuromusculares só têm realmente tratamentos paliativos, onde só podem retardar a gravidade de alguns dos sintomas. Não há realmente uma boa maneira de reverter ou prevenir os danos.” Disse Santoso. “Fazer esses tipos de modelos e tentar analisar os mecanismos da doença pode nos dar uma ideia melhor de como podemos desenvolver terapêuticas para aliviar melhor os sintomas ou, idealmente, removê-los.”
Publicado em 18/09/2021 09h45
Artigo original:
Estudo original:


