A terapia com células T CAR, o método inovador de sobrecarregar as células T dos pacientes no laboratório para atacar o câncer quando reinfundida, funcionou de forma mais eficaz contra os cânceres do sangue do que os tumores sólidos.
Agora, em uma nova pesquisa destinada a descobrir por que e como superar o problema em tumores sólidos, cientistas em Milão, Itália, descobriram que os tumores sólidos se protegem em um revestimento de açúcar que os torna resistentes ao ataque de células T CAR. Beatrice Greco e colegas da Unidade de Imunoterapias Inovadoras do Instituto Científico IRCCS San Raffaele estão explorando maneiras de superá-lo. Eles estão criando um torpedo molecular que pode quebrar o escudo de açúcar, o que, por sua vez, abre caminho para as células T CAR se instalarem e destruirem cânceres sólidos.
As células T CAR ? células T receptoras de antígenos quiméricos ? começam como células T do próprio paciente isoladas de uma amostra de sangue. Em seguida, as células são preparadas em laboratório usando um processo de modificação genética que faz com que as células T expressem um receptor de busca e destruição do câncer em sua superfície.
Apesar de muitos anos de pesquisa, os cientistas médicos não foram capazes de persuadir as células T supercarregadas a funcionar tão eficientemente contra tumores sólidos quanto para malignidades hematológicas. E a glicosilação da superfície da célula cancerosa, o processo de as células cancerígenas se fortalecerem em uma espessa camada de moléculas de açúcar, levou a dificuldades no uso do CAR T contra uma variedade de tumores sólidos.
Estudos de laboratório envolvendo modelos animais sugerem que uma solução para o problema do açúcar pode entrar em testes clínicos em humanos em um futuro não muito distante.
“A imunoterapia com células T projetadas para receptores de antígenos quiméricos mostrou sucessos excepcionais em pacientes com malignidades de células B refratárias”, escreveu Greco na Science Translational Medicine. “No entanto, os primeiros estudos em humanos em tumores sólidos revelaram obstáculos únicos que contribuem para a fraca demonstração de eficácia. Compreender os determinantes do reconhecimento do tumor por células T CAR deve traduzir-se na concepção de estratégias que podem superar a resistência.”
Não é apenas um problema de açúcar que impede a terapia com células T CAR de funcionar em tumores sólidos, embora o revestimento de carboidratos tenha sido a maior barreira para o sucesso do tratamento. O microambiente de tumores sólidos auxilia na prevenção de células T CAR de se infiltrarem adequadamente no local do tumor. Além disso, os tumores sólidos também possuem poucos antígenos que as células T CAR podem reconhecer prontamente e se concentrar.
Pesquisadores em todo o mundo estão trabalhando em maneiras de superar essas barreiras, mas é necessário mais trabalho para entender os fatores que influenciam se uma célula T CAR pode reconhecer e interagir com seu alvo maligno, dizem cientistas em Milão.
Para saber por que praticamente todo tipo de tumor sólido é resistente à terapia com células T CAR, Greco e seus colegas procuraram o que esses cânceres tinham em comum quando se trata de células que se protegem contra a destruição. A equipe descobriu que “múltiplos carcinomas expressam N-glicanos extracelulares, cuja abundância se correlaciona negativamente com a morte de células T CAR”.
A glicosilação ligada a N refere-se a um processo químico crucial no qual uma oligossacariltransferase (uma enzima) catalisa a transferência de um oligossacarídeo para um aceptor de aminoácidos, que neste caso é a asparagina. Um oligossacarídeo é um carboidrato composto por uma série de subunidades de monossacarídeos.
Imagine isso como um processo de construção de uma cadeia com várias unidades, ligando-se repetidamente. Cada vez que um oligossacarídeo se liga a uma asparagina exposta, esse é outro elo da cadeia. O resultado final é uma cadeia apertada de moléculas de açúcar que construíram uma fortaleza nas células cancerígenas. No nível macro, o tumor é protegido em açúcares que mantêm o câncer livre de ataques. Greco e colegas dizem que a glicosilação ligada a N é a chave para a resistência dos tumores sólidos à imunoterapia com células T CAR.
Ao incluir um análogo de açúcar – uma molécula anti-açúcar que serve como um torpedo – junto com as células T CAR, o poder de matar das células T estimuladas pode ser aprimorado, descobriram Greco e colegas. E como as células cancerígenas têm uma infinidade de métodos para evitar qualquer forma de tratamento, ela e sua equipe dizem que incorporar a molécula anti-açúcar nos tratamentos com células T CAR pode ajudar a superar vários truques que os tumores podem usar para se proteger.
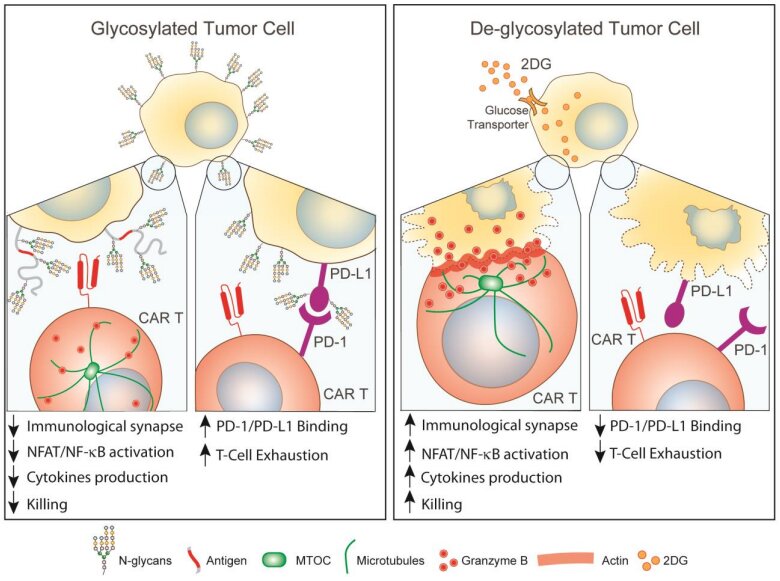
“Mostramos que os N-glicanos protegem os tumores da morte de células T CAR, interferindo na formação adequada de sinapses imunológicas e reduzindo a ativação transcricional, a produção de citocinas e a citotoxicidade”, escreveu Greco. “Para superar essa barreira, exploramos a alta demanda metabólica dos tumores para inibir com segurança a síntese de N-glicanos”.
As células pancreáticas protegem-se generosamente dos compostos de carboidratos ? N-glicanos ? em sua superfície. Os N-glicanos funcionam como um campo de força contra as células T CAR no câncer de pâncreas. A malignidade é um dos cânceres mais difíceis de tratar. Ser capaz de usar a imunoterapia com células T CAR pode adicionar ao arsenal que os médicos podem um dia confiar.
Para resolver o problema do revestimento de açúcar, a equipe usou um torpedo molecular ? uma 2-desoxi-D-glicose ? um análogo de açúcar que pode inibir a síntese de N-glicanos. Os pesquisadores descobriram que o tratamento de tumores pancreáticos em camundongos com 2-desoxi-D-glicose quebrou as células tumorais que revestem o escudo de N-glicano, deixando-as mais vulneráveis à terapia com células T CAR.
Além disso, o tratamento combinado (2-desoxi-D-glicose mais imunoterapia com células T CAR) também sensibilizou uma série de outros tumores sólidos à terapia com células T CAR. Esses tumores sólidos incluíam câncer de pulmão, ovário e bexiga.
Enquanto pesquisadores em Milão e além estão trabalhando em maneiras de superar as barreiras à capacidade das células T CAR de destruir cânceres, é necessário mais trabalho para entender os fatores que influenciam se uma célula T CAR pode reconhecer e interagir com seu alvo maligno.
Mesmo entre os cânceres hematológicos, as estimativas de uma enxurrada de estudos recentes sugerem que a terapia com células T CAR tem apenas uma taxa de sucesso de 30 a 40% para remissão durável. Isso significa que um número significativo de pacientes não está se beneficiando da promessa do tratamento.
Para melhorar as chances, cientistas médicos em laboratórios em todo o mundo estão procurando maneiras de fazer a terapia do câncer com células T CAR funcionar de forma mais eficiente para cânceres hematológicos e sólidos.
“No geral, nossos resultados indicam que a N-glicosilação do tumor regula a qualidade e a magnitude das respostas das células T CAR, abrindo caminho para o design racional de terapias aprimoradas contra malignidades sólidas”, disse Greco.
Publicado em 26/03/2022 13h27
Artigo original:
Estudo original:


