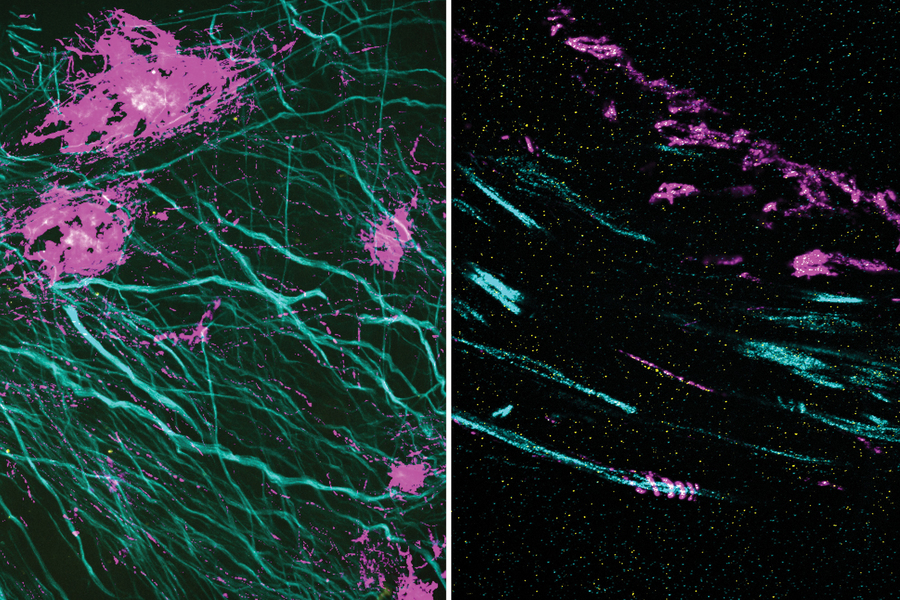
Créditos: Imagem: Zhuyu Peng e Jinyoung Kang
Separar moléculas densamente compactadas antes da imagem permite que elas se tornem visíveis pela primeira vez.
Dentro de uma célula viva, as proteínas e outras moléculas são muitas vezes compactadas. Esses aglomerados densos podem ser difíceis de visualizar porque os rótulos fluorescentes usados para torná-los visíveis não podem se encaixar entre as moléculas.
Os pesquisadores do MIT agora desenvolveram uma nova maneira de superar essa limitação e tornar visíveis essas moléculas “invisíveis”. Sua técnica permite que eles “desagrupem” as moléculas expandindo uma amostra de célula ou tecido antes de rotular as moléculas, o que torna as moléculas mais acessíveis a marcadores fluorescentes.
Este método, que se baseia em uma técnica amplamente utilizada conhecida como microscopia de expansão desenvolvida anteriormente no MIT, deve permitir que os cientistas visualizem moléculas e estruturas celulares que nunca foram vistas antes.
“Está ficando claro que o processo de expansão revelará muitas novas descobertas biológicas. Se biólogos e clínicos estudam uma proteína no cérebro ou outro espécime biológico, e estão rotulando-a da maneira regular, podem estar perdendo categorias inteiras de fenômenos”, diz Edward Boyden, professor de neurotecnologia da Y. Eva Tan, professor de engenharia biológica e ciências cerebrais e cognitivas no MIT, pesquisador do Howard Hughes Medical Institute e membro do McGovern Institute for Brain Research do MIT e do Koch Institute for Integrative Cancer Research.
Usando essa técnica, Boyden e seus colegas mostraram que podiam imaginar uma nanoestrutura encontrada nas sinapses dos neurônios. Eles também visualizaram a estrutura das placas beta-amiloides ligadas à doença de Alzheimer com mais detalhes do que era possível antes.
“Nossa tecnologia, que chamamos de revelação de expansão, permite a visualização dessas nanoestruturas, que antes permaneciam ocultas, usando hardware facilmente disponível em laboratórios acadêmicos”, diz Deblina Sarkar, professora assistente do Media Lab e uma das principais autoras do estudo.
Os autores seniores do estudo são Boyden; Li-Huei Tsai, diretor do Instituto Picower para Aprendizagem e Memória do MIT; e Thomas Blanpied, professor de fisiologia da Universidade de Maryland. Outros autores principais incluem Jinyoung Kang, um pós-doutorado do MIT, e Asmamaw Wassie, um recente destinatário de PhD do MIT. O estudo aparece hoje na Nature Biomedical Engineering.
Despovoamento
A imagem de uma proteína específica ou outra molécula dentro de uma célula requer rotulá-la com uma etiqueta fluorescente transportada por um anticorpo que se liga ao alvo. Os anticorpos têm cerca de 10 nanômetros de comprimento, enquanto as proteínas celulares típicas geralmente têm cerca de 2 a 5 nanômetros de diâmetro, portanto, se as proteínas alvo estiverem muito densamente compactadas, os anticorpos não poderão alcançá-las.
Isso tem sido um obstáculo para a imagem tradicional e também para a versão original da microscopia de expansão, que Boyden desenvolveu pela primeira vez em 2015. Na versão original da microscopia de expansão, os pesquisadores anexaram rótulos fluorescentes a moléculas de interesse antes de expandir o tecido. A marcação foi feita primeiro, em parte porque os pesquisadores tiveram que usar uma enzima para cortar proteínas na amostra para que o tecido pudesse ser expandido. Isso significava que as proteínas não podiam ser rotuladas após o tecido ser expandido.
Para superar esse obstáculo, os pesquisadores tiveram que encontrar uma maneira de expandir o tecido, deixando as proteínas intactas. Eles usaram calor em vez de enzimas para amolecer o tecido, permitindo que o tecido se expandisse 20 vezes sem ser destruído. Então, as proteínas separadas podem ser marcadas com marcadores fluorescentes após a expansão.
Com tantas outras proteínas acessíveis para rotulagem, os pesquisadores foram capazes de identificar pequenas estruturas celulares dentro das sinapses, as conexões entre os neurônios que são densamente embalados com proteínas. Eles rotularam e visualizaram sete proteínas sinápticas diferentes, o que lhes permitiu visualizar, em detalhes, “nanocolunas” consistindo de canais de cálcio alinhados com outras proteínas sinápticas. Essas nanocolunas, que se acredita ajudar a tornar a comunicação sináptica mais eficiente, foram descobertas pelo laboratório de Blanpied em 2016.
“Esta tecnologia pode ser usada para responder a muitas questões biológicas sobre disfunção em proteínas sinápticas, que estão envolvidas em doenças neurodegenerativas”, diz Kang. “Até agora não havia nenhuma ferramenta para visualizar as sinapses muito bem.”
Novos padrões
Os pesquisadores também usaram sua nova técnica para obter imagens de beta-amilóide, um peptídeo que forma placas nos cérebros de pacientes com Alzheimer. Usando tecido cerebral de camundongos, os pesquisadores descobriram que a beta-amiloide forma nanoaglomerados periódicos, que não haviam sido vistos antes. Esses aglomerados de beta-amiloide também incluem canais de potássio. Os pesquisadores também encontraram moléculas beta-amiloides que formavam estruturas helicoidais ao longo dos axônios.
“Neste artigo, não especulamos sobre o que essa biologia pode significar, mas mostramos que ela existe. Esse é apenas um exemplo dos novos padrões que podemos ver”, diz Margaret Schroeder, estudante de pós-graduação do MIT que também é autora do artigo.
Sarkar diz que está fascinada pelos padrões biomoleculares em nanoescala que essa tecnologia revela. “Com formação em nanoeletrônica, desenvolvi chips eletrônicos que exigem alinhamento extremamente preciso, na nanofabricação. Mas quando vejo que em nosso cérebro a Mãe Natureza organizou biomoléculas com tanta precisão em nanoescala, isso realmente me impressiona”, diz ela.
Boyden e os membros de seu grupo agora estão trabalhando com outros laboratórios para estudar estruturas celulares, como agregados de proteínas ligados ao Parkinson e outras doenças. Em outros projetos, eles estão estudando patógenos que infectam células e moléculas envolvidas no envelhecimento cerebral. Os resultados preliminares desses estudos também revelaram novas estruturas, diz Boyden.
“Repetidas vezes, você vê coisas que são realmente chocantes”, diz ele. “Isso nos mostra o quanto estamos perdendo com a coloração clássica não expandida.”
Os pesquisadores também estão trabalhando na modificação da técnica para que possam visualizar até 20 proteínas por vez. Eles também estão trabalhando na adaptação de seu processo para que possa ser usado em amostras de tecidos humanos.
Sarkar e sua equipe, por outro lado, estão desenvolvendo minúsculos dispositivos nanoeletrônicos sem fio que podem ser distribuídos no cérebro. Eles planejam integrar esses dispositivos com revelação de expansão. “Isso pode combinar a inteligência da nanoeletrônica com a proeza da nanoscopia da tecnologia de expansão, para uma compreensão funcional e estrutural integrada do cérebro”, diz Sarkar.
Publicado em 30/08/2022 12h56
Artigo original:


