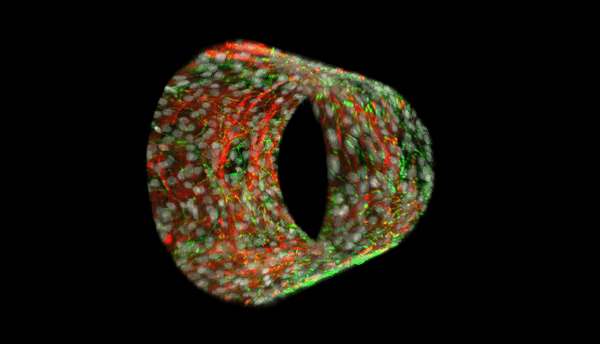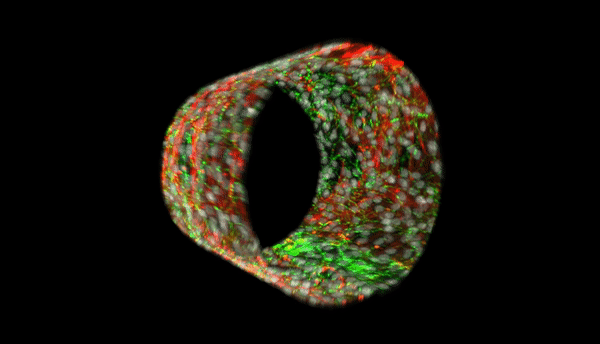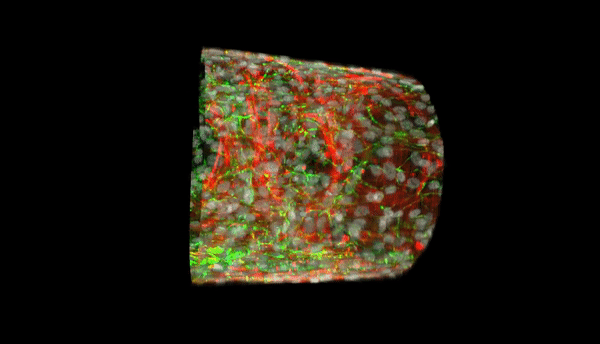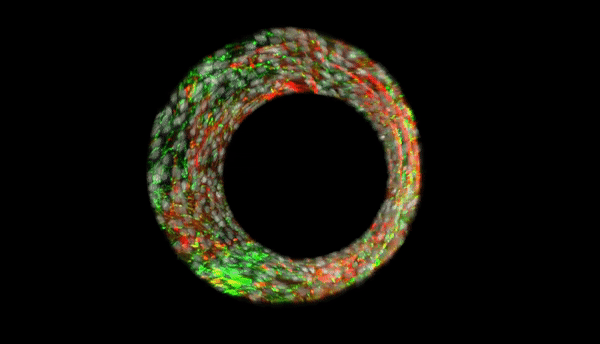
Durante a progressão da hipertensão pulmonar, as alterações estruturais e funcionais nas pequenas artérias musculares desempenham um papel significativo e contribuem para a doença. Os bioengenheiros pretendem desenvolver modelos avançados de microvasos anatomicamente biomiméticos in vitro, uma vez que os vasos não humanos não são uma representação precisa da arquitetura microvascular e do microambiente humanos. Em um novo relatório agora no Science Advances, Qianru Jin e uma equipe de pesquisa multidisciplinar da Universidade Johns Hopkins, EUA, descreveram um novo método para a biofabricação paralela de um microvaso arterial pulmonar fotopatizado, autolaminado e biomimético de tamanho e arquitetura ajustáveis.
As características dos microvasos eram anatomicamente precisas com camadas e padronização de células musculares lisas humanas alinhadas, matriz extracelular e células endoteliais. As estruturas exibiram uma longevidade notavelmente aumentada nas células endoteliais e produziram óxido nítrico. Os cientistas usaram o processamento computacional de imagens para obter simulações bidimensionais de alta resolução de células e proteínas. O novo trabalho fornece um modelo completo para a bioengenharia de tecidos multicelulares com base no posicionamento espacial preciso tridimensional (3-D). A nova plataforma biomimética permitirá que pesquisadores médicos investigem a patobiologia microvascular em doenças humanas.
Nas principais doenças cardiovasculares (DCV), incluindo doenças cardíacas pulmonares, a desregulação do tônus vasomotor nos vasos arteriais pode aumentar a resistência periférica. Os pesquisadores usam o termo “pequenas artérias pulmonares musculares” humanas (hSMPA) para descrever os vasos de resistência à microvasculatura no lado da oferta durante a circulação pulmonar humana. Esses vasos são equivalentes às artérias durante a circulação sistêmica. Enquanto os modelos existentes em laboratório não resumem adequadamente a complexidade da vasculatura, os modelos animais de DCV também são limitados, pois se desviam da infraestrutura vascular humana. Os modelos in vitro inspirados em tecidos microvasculares fornecerão maior eficiência durante pesquisas básicas e translacionais para avançar na fisiopatologia das DCV. Por exemplo, os engenheiros de tecidos desenvolveram sistemas tecido em um chip ou órgão em um chip para combinar cultura celular com microfluídica para imitar ambientes fisiológicos e fornecer pistas para investigar a fisiopatologia e a descoberta ou desenvolvimento de medicamentos. No entanto, os chips fluidos microfabricados não podem recapitular a morfologia nativa dos microvasos e requerem máquinas especiais para produção em escala ampliada. Para abordar esses limites existentes, Jin et al. criaram construções biomiméticas com características essenciais de hSMPAs (pequenas artérias pulmonares musculares humanas).
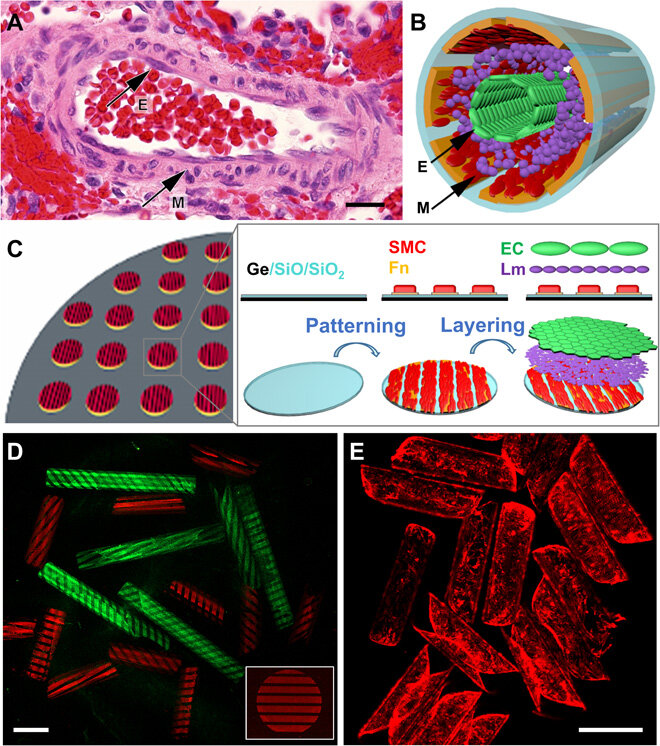
Para obter camadas anatomicamente corretas, os cientistas se concentraram no alinhamento das células do músculo liso vascular (VSMC) e nos padrões de crescimento como características-chave durante a patogênese da hipertensão pulmonar. A abordagem para projetar a citoarquitetura precisa para hSMPAs garantiu uma biomimética precisa do modelo para testar e recapitular a fisiopatologia da doença. A equipe usou fotolitografia e deposição de filmes finos biocompatíveis para padronizar com precisão as células humanas e recapitular a microarquitetura da parede do vaso.
Bioengenharia da artéria pulmonar muscular pequena humana biomimética (hSMPA)
A equipe de pesquisa combinou os principais recursos dos hSMPAs, incluindo diâmetros variando de 50 a 300 µm, um revestimento íntimo confluente de células endoteliais (CE) e uma população alinhada de VSMC (células do músculo liso vascular). Eles então projetaram uma bicamada de dupla camada de monóxido de silício / dióxido de silício (SiO / SiO2) na escala de wafer e incorporaram fotolitografia, deposição física de vapor e padronização de proteínas durante o trabalho. O dióxido de silício foi passível de modificação da superfície, permitindo padronizar as proteínas da matriz na superfície luminal das construções tubulares. Jin et al. usou germânio (Ge) sob a bicamada SiO / SiO2 como uma construção amiga da célula para evitar a necessidade de produtos químicos agressivos durante a montagem da artéria pulmonar. A superfície proporcionou descolamento ajustável para otimizar a adesão das camadas celulares constituintes e obter cobertura celular uniforme durante os experimentos.
Considerações mecânicas para construções tubulares e caracterização da cobertura celular
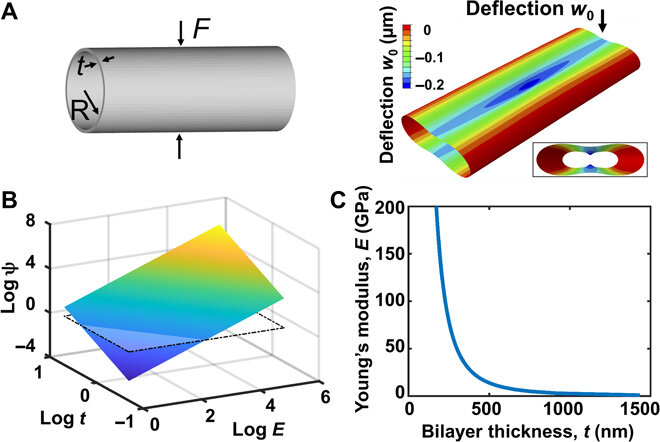
A equipe então desenvolveu um modelo mecânico e incluiu o módulo de elasticidade (razão de tensão e deformação), espessura do substrato e raio de curvatura para estudar a rigidez das células da parede vascular expostas às construções tubulares. Os módulos elásticos de SiO e SiO2 excederam o da parede arterial pulmonar nativa em seis ordens de magnitude. Para modelar a rigidez à flexão à qual as células são expostas em seu ambiente nativo, Jin et al. então considerado um modelo teórico. Utilizando análise de elementos finitos, eles verificaram a lei de escala teórica e testaram a constante de proporcionalidade que representa a tração celular. Com base na análise de escala, as construções tubulares de SiO / SiO2 aproximaram a micromecânica da parede hSMPA, enquanto a rigidez à flexão das construções biodegradáveis eventualmente se assemelhou ao estado nativo, permitindo maior biocompatibilidade dos materiais.
Após 48 horas de semeadura de células endoteliais microvasculares pulmonares humanas (HPMECs) nas construções, eles observaram uma monocamada confluente de células na superfície luminal do microvaso biomimético. Eles não conseguiram visualizar a imagem de todo o microvaso biomimético 3D devido à profundidade e curvatura da estrutura, abordadas por meio de um suporte correspondente de índice de refração. Depois disso, eles obtiveram imagens sequenciais de cada lado da amostra para obter uma pilha z de todo o tubo para visualização em 3D.
HPMECs de co-cultura e células do músculo liso da artéria pulmonar humana (HPASMCs).
Para imitar a estrutura e a composição das pequenas artérias pulmonares musculares humanas, a equipe semeou células do músculo liso da artéria pulmonar humana (HPASMCs) sobre a bicamada do material e depois depositou a laminina – um componente importante da lâmina elástica interna. Eles observaram camadas distintas e anatomicamente corretas dos dois tipos de células em alta resolução em 3-D. As células do músculo liso vascular (VSMCs) na camada medial das pequenas artérias pulmonares musculares humanas (hSMPA) são tipicamente dispostas circunferencialmente para afetar o fluxo microvascular pulmonar e a vasorreatividade. No entanto, os modelos computacionais são incapazes de capturar esse alinhamento ou permitir a sintonização para abordar efetivamente a importância das VSMCs na citoarquitetura hSMPA ou suas contribuições para a resistência vascular pulmonar. Jin et al. portanto, utilizou litografia e fibronectina padronizada nos filmes antes de liberar e rolar os microvasos biomiméticos. O trabalho permitiu que eles observassem a integridade do padrão a ser preservado. Quando os cientistas cultivaram HPASMCs nessas superfícies, as células demonstraram alta fidelidade e alinhamento celular anatomicamente preciso. Portanto, a equipe introduzirá a direcionalidade controlada dos padrões, adicionando condições de contorno através de tais designs de máscara no futuro.
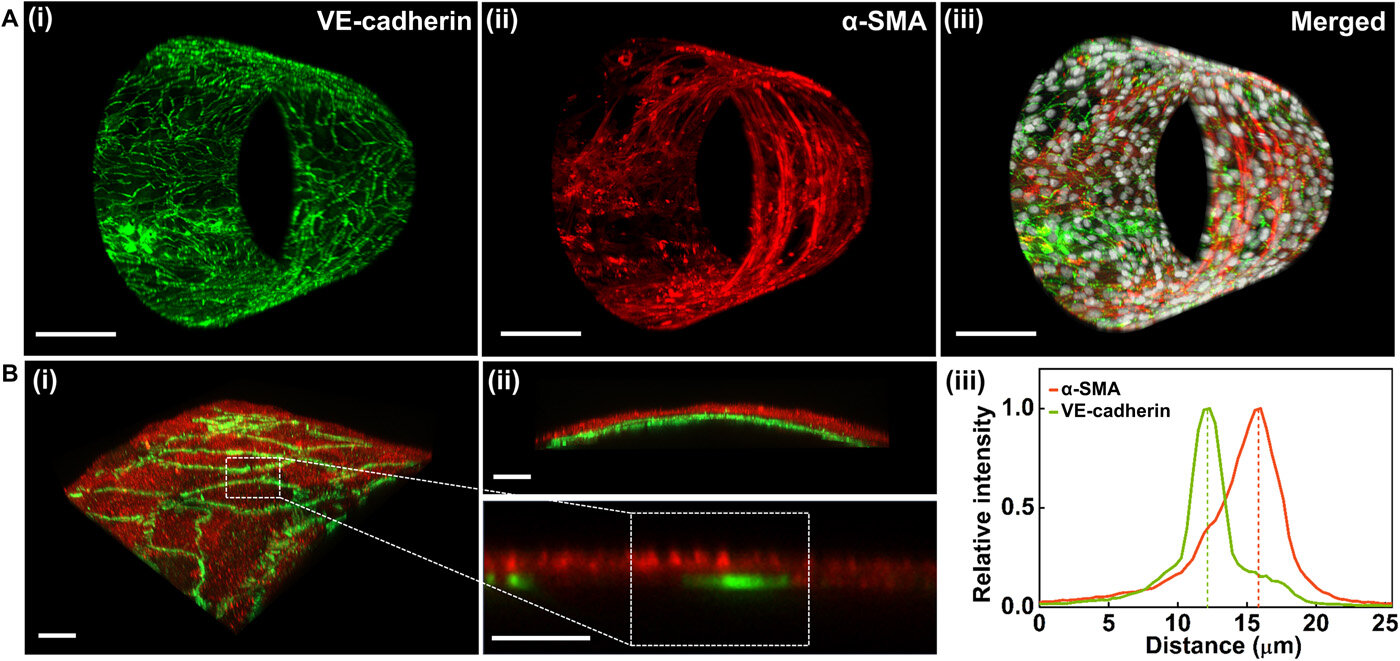
Melhor longevidade celular e sinalização em artérias pulmonares biomiméticas
Como a viabilidade celular a longo prazo é importante na engenharia de tecidos, a equipe de pesquisa observou células endoteliais (HPMECs) e células musculares lisas (HPASMCs) co-cultivadas nas artérias pulmonares biomiméticas (hSMPA) para demonstrar uma longevidade substancial. Os HPMECs também mostraram produção substancial de óxido nítrico nos vasos biomiméticos, que aumentaram quatro vezes em 48 horas em comparação com as células de controle cultivadas em filmes planos de SiO / SiO2. Os dados mostraram como as artérias pulmonares biomiméticas aumentaram a função robusta das células da parede vascular.

Dessa maneira, Qianru Jin e seus colegas desenvolveram construções ajustáveis, auto-dobráveis e de produção em massa que permitiam camadas multicelulares precisas para maior viabilidade e funcionalidade das células vasculares pulmonares humanas no laboratório. A equipe descreveu a primeira abordagem integrada para padronizar, gerar, criar imagens e analisar funções celulares e teciduais microalinhadas e em camadas nas artérias pulmonares biomiméticas in vitro. O trabalho fornece um passo importante para formar uma plataforma in vitro e estudar a biologia da parede vascular em um ambiente específico de tecido humano anatomicamente preciso. Os cientistas esperam que a nova abordagem forneça informações para entender doenças cardiovasculares e outros desafios prementes da saúde pública baseados em microvasculares.
Publicado em 04/04/2020 14h29
Artigo original:
Achou importante? Compartilhe!
Assine nossa newsletter e fique informado sobre Astrofísica, Biofísica, Geofísica e outras áreas. Preencha seu e-mail no espaço abaixo e clique em “OK”:




