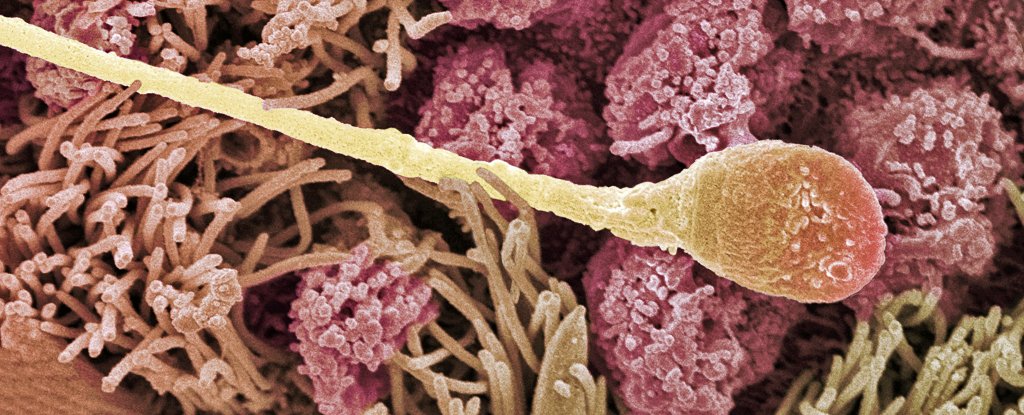
Estudos em mamíferos mostraram que as ‘memórias’ de vários efeitos ambientais – como dieta, peso e estresse – estão sendo passadas de pais para filhos, apesar desses estados não serem codificados nas sequências de DNA transportadas pelos espermatozoides. Agora, temos uma nova explicação de como isso é possível.
A história tem muito a ver com epigenética. Moléculas que se ligam ao DNA podem atuar como interruptores que controlam quais seções do DNA são usadas – mas até agora não sabíamos quais dessas moléculas podem carregar as configurações marcadas pelas experiências de vida de um pai, para serem incorporadas a um embrião via esperma.
“O grande avanço com este estudo é que ele identificou um meio não baseado em DNA pelo qual os espermatozoides se lembram do ambiente do pai (dieta) e transmitem essa informação ao embrião”, disse a epigeneticista Sarah Kimmins da Universidade McGill.
Usando ratos, a epigeneticista Ariane Lismer e colegas foram capazes de demonstrar que os efeitos de uma dieta deficiente em folato podem ser transmitidos pela alteração das moléculas de histonas no esperma. Simplificando, as histonas são proteínas realmente básicas que o DNA enrola para armazenamento sem emaranhados.
Nos mamíferos, quando os corpos masculinos constroem esperma, eles jogam fora a maior parte dos carretéis de histona, para permitir um empacotamento mais apertado.
Mas uma pequena porcentagem ainda permanece (1 por cento em camundongos e 15 por cento em humanos), fornecendo estrutura para o DNA em regiões específicas para a criação e função do esperma, metabolismo e desenvolvimento do embrião – para permitir que os mecanismos celulares façam uso dessas instruções do DNA.
A modificação química dessas histonas – a forma mais comum sendo a metilação – é o que permite ou impede que o DNA seja “lido” para que possa ser transcrito em produtos proteicos. Uma dieta pobre pode fazer com que essas histonas mudem seu estado de metilação.
É por isso que ouvimos sobre a importância do folato para as mulheres durante a gravidez: o folato da mãe ajuda a estabilizar a metilação do DNA em seus filhotes.
Ao alimentar ratos machos com uma dieta deficiente em folato desde o momento em que foram desmamados, os pesquisadores foram capazes de rastrear as mudanças nas histonas do esperma do macho e nos embriões resultantes. E, de fato, alterações na histona dos espermatozoides também estavam presentes no embrião em desenvolvimento.
“Ninguém foi capaz de rastrear como essas assinaturas ambientais hereditárias são transmitidas do esperma para o embrião antes”, disse Lismer.
A equipe também descobriu que esses efeitos podem ser cumulativos e levar a um aumento na gravidade dos defeitos de nascença.
Curiosamente, os defeitos congênitos vistos nos camundongos, incluindo subdesenvolvimento no nascimento e anormalidades da coluna vertebral, estão bem documentados em populações humanas com deficiência de folato.
Os pesquisadores esperam que a expansão do nosso conhecimento sobre os mecanismos de herança revele novas maneiras de tratar e prevenir essas condições. Mas há muito mais para trabalhar antes disso.
“Nossos próximos passos serão determinar se essas alterações prejudiciais induzidas nas proteínas do esperma (histonas) podem ser reparadas. Temos novos trabalhos interessantes que sugerem que este é realmente o caso”, disse Kimmins.
Publicado em 21/03/2021 12h25
Artigo original:
Estudo original:


