
Pode parecer surpreendente, mas quando os tempos são difíceis e não há outro alimento disponível, algumas bactérias do solo podem consumir vestígios de hidrogênio no ar como fonte de energia.
Na verdade, as bactérias removem anualmente 70 milhões de toneladas de hidrogênio da atmosfera, um processo que literalmente molda a composição do ar que respiramos.
Isolamos uma enzima que permite que algumas bactérias consumam hidrogênio e extraiam energia dele, e descobrimos que ela pode produzir uma corrente elétrica diretamente quando exposta a quantidades mínimas de hidrogênio.
Como relatamos em um novo artigo na Nature, a enzima pode ter um potencial considerável para alimentar pequenos dispositivos movidos a ar sustentáveis no futuro.
Genes bacterianos contêm o segredo para transformar ar em eletricidade
Impulsionados por essa descoberta, analisamos o código genético de uma bactéria do solo chamada Mycobacterium smegmatis, que consome hidrogênio do ar.
Escrito nesses genes está o projeto para produzir a máquina molecular responsável por consumir hidrogênio e convertê-lo em energia para a bactéria. Esta máquina é uma enzima chamada “hidrogenase”, e nós a chamamos de Huc para abreviar.
O hidrogênio é a molécula mais simples, feita de dois prótons carregados positivamente mantidos juntos por uma ligação formada por dois elétrons carregados negativamente. Huc quebra essa ligação, os prótons se separam e os elétrons são liberados.
Nas bactérias, esses elétrons livres fluem para um circuito complexo chamado “cadeia de transporte de elétrons” e são aproveitados para fornecer energia à célula.
Elétrons fluindo são o que a eletricidade é feita, o que significa que Huc converte diretamente o hidrogênio em corrente elétrica.
O hidrogênio representa apenas 0,00005% da atmosfera. Consumir esse gás nessas baixas concentrações é um desafio formidável, que nenhum catalisador conhecido pode alcançar. Além disso, o oxigênio, que é abundante na atmosfera, envenena a atividade da maioria dos catalisadores que consomem hidrogênio.
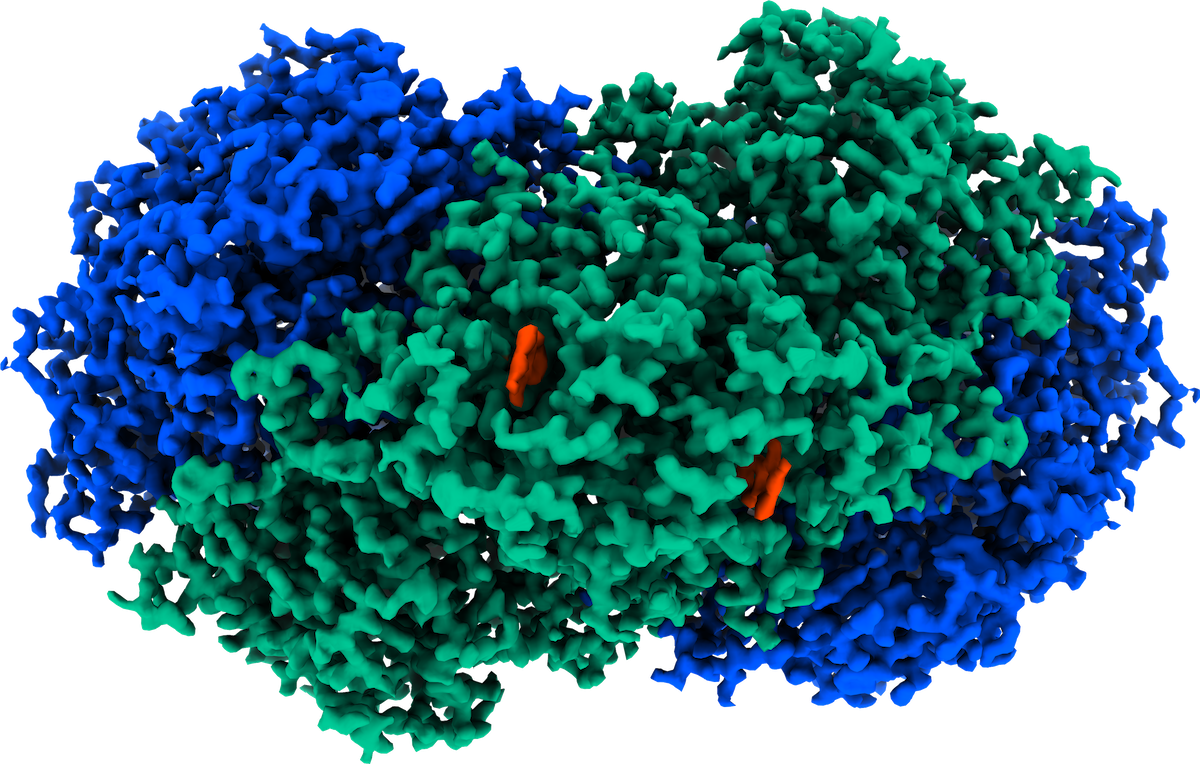
Isolando a enzima que permite que as bactérias vivam no ar
Queríamos saber como o Huc supera esses desafios, então decidimos isolá-lo das células de M. smegmatis.
O processo para fazer isso foi complicado. Primeiro modificamos os genes em M. smegmatis que permitem que a bactéria produza essa enzima. Ao fazer isso, adicionamos uma sequência química específica ao Huc, o que nos permitiu isolá-lo das células de M. smegmatis.
Dar uma boa olhada em Huc não foi fácil. Demorou vários anos e alguns becos sem saída experimentais antes de finalmente isolarmos uma amostra de alta qualidade da engenhosa enzima.
No entanto, o trabalho árduo valeu a pena, pois o Huc que eventualmente produzimos é muito estável. Ele resiste a temperaturas de 80 – até -80 – sem perda de atividade.
O projeto molecular para extrair hidrogênio do ar
Com o Huc isolado, começamos a estudá-lo seriamente, para descobrir do que exatamente a enzima é capaz. Como ele pode transformar o hidrogênio do ar em uma fonte sustentável de eletricidade?
Notavelmente, descobrimos que, mesmo quando isolado da bactéria, o Huc pode consumir hidrogênio em concentrações muito mais baixas do que os minúsculos vestígios no ar. Na verdade, Huc ainda consumia cheiros de hidrogênio muito fracos para serem detectados por nosso cromatógrafo a gás, um instrumento altamente sensível que usamos para medir as concentrações de gás.
Também descobrimos que o Huc é totalmente desinibido pelo oxigênio, uma propriedade não vista em outros catalisadores que consomem hidrogênio.
Para avaliar sua capacidade de converter hidrogênio em eletricidade, usamos uma técnica chamada eletroquímica. Isso mostrou que o Huc pode converter concentrações mínimas de hidrogênio no ar diretamente em eletricidade, que pode alimentar um circuito elétrico. Esta é uma conquista notável e sem precedentes para um catalisador que consome hidrogênio.
Usamos vários métodos de ponta para estudar como o Huc faz isso no nível molecular. Estes incluíram microscopia avançada (microscopia eletrônica criogênica) e espectroscopia para determinar sua estrutura atômica e vias elétricas, ultrapassando os limites para produzir a estrutura enzimática mais altamente resolvida já relatada por este método.

As enzimas podem usar o ar para alimentar os dispositivos de amanhã
Ainda é cedo para esta pesquisa, e vários desafios técnicos precisam ser superados para realizar o potencial do Huc.
Por um lado, precisaremos aumentar significativamente a escala de produção de Huc. No laboratório, produzimos Huc em quantidades de miligramas, mas queremos escalar isso para gramas e, por fim, quilogramas.
No entanto, nosso trabalho demonstra que o Huc funciona como uma “bateria natural” produzindo uma corrente elétrica sustentada do ar ou hidrogênio adicionado.
Como resultado, o Huc tem um potencial considerável no desenvolvimento de dispositivos pequenos e sustentáveis movidos a ar como alternativa à energia solar.
A quantidade de energia fornecida pelo hidrogênio no ar seria pequena, mas provavelmente suficiente para alimentar um monitor biométrico, relógio, globo de LED ou computador simples. Com mais hidrogênio, o Huc produz mais eletricidade e pode alimentar dispositivos maiores.
Outra aplicação seria o desenvolvimento de sensores bioelétricos baseados em Huc para detectar hidrogênio, que podem ser incrivelmente sensíveis. O Huc pode ser inestimável para detectar vazamentos na infraestrutura de nossa crescente economia de hidrogênio ou em um ambiente médico.
Em suma, esta pesquisa mostra como uma descoberta fundamental sobre como as bactérias nos solos se alimentam pode levar a uma reimaginação da química da vida. Em última análise, também pode levar ao desenvolvimento de tecnologias para o futuro.
Publicado em 13/03/2023 07h58
Artigo original:


