O transtorno de estresse pós-traumático (TEPT) é uma condição de saúde mental difícil de curar causada pela experiência de um evento traumatizante, como violência interpessoal ou desastre. Embora os sofredores de TEPT tenham existido em toda a história humana e a condição seja observada em animais, o diagnóstico dessa condição só apareceu na década de 1970 após a Guerra do Vietnã. Pacientes com TEPT são amplamente conhecidos por sofrerem de vários sintomas de flashbacks recorrentes, ansiedade e alteração negativa na cognição.
Atualmente, várias opções de tratamento, como antidepressivos ou terapia cognitivo-comportamental, são usadas para tratar o TEPT. Os inibidores seletivos da recaptação da serotonina (ISRSs) são a única classe de antidepressivos aprovados para o tratamento do TEPT. No entanto, os medicamentos apresentam desvantagens de ação retardada e não são eficazes em alguns pacientes.
Terapias cognitivo-comportamentais, como dessensibilização e reprocessamento por movimentos oculares (EMDR), também são frequentemente usadas para tratar o TEPT. No entanto, essas terapias de extinção do medo não são eficazes em metade dos pacientes. Além disso, mesmo quando a terapia é bem-sucedida, o TEPT é notório pela recorrência dos sintomas. Essa recaída do TEPT tratado anteriormente é chamada de “recuperação espontânea”, que é objeto de muitos estudos.
No passado, estudos apontaram que as atividades nos neurônios glutamatérgicos são uma parte importante da fisiopatologia do TEPT. Particular interesse está nos efeitos do receptor N-metil-D-aspartato (NMDAR) sobre esses neurônios, que é responsável pelo controle da plasticidade sináptica relacionada ao aprendizado e à memória.
Para combater o TEPT em suas raízes, os pesquisadores do Centro de Cognição e Socialidade do Instituto de Ciências Básicas (IBS), em conjunto com a Universidade de Yale, exploraram o mecanismo molecular do tratamento do TEPT. Em sua pesquisa mais recente, publicada na Molecular Psychiatry, a equipe do IBS testou um medicamento de teste de TEPT chamado NYX-783 em camundongos e examinou o mecanismo molecular de suas ações. NYX-783 é uma droga recém-descoberta que é conhecida por modular as funções NMDAR nos neurônios.
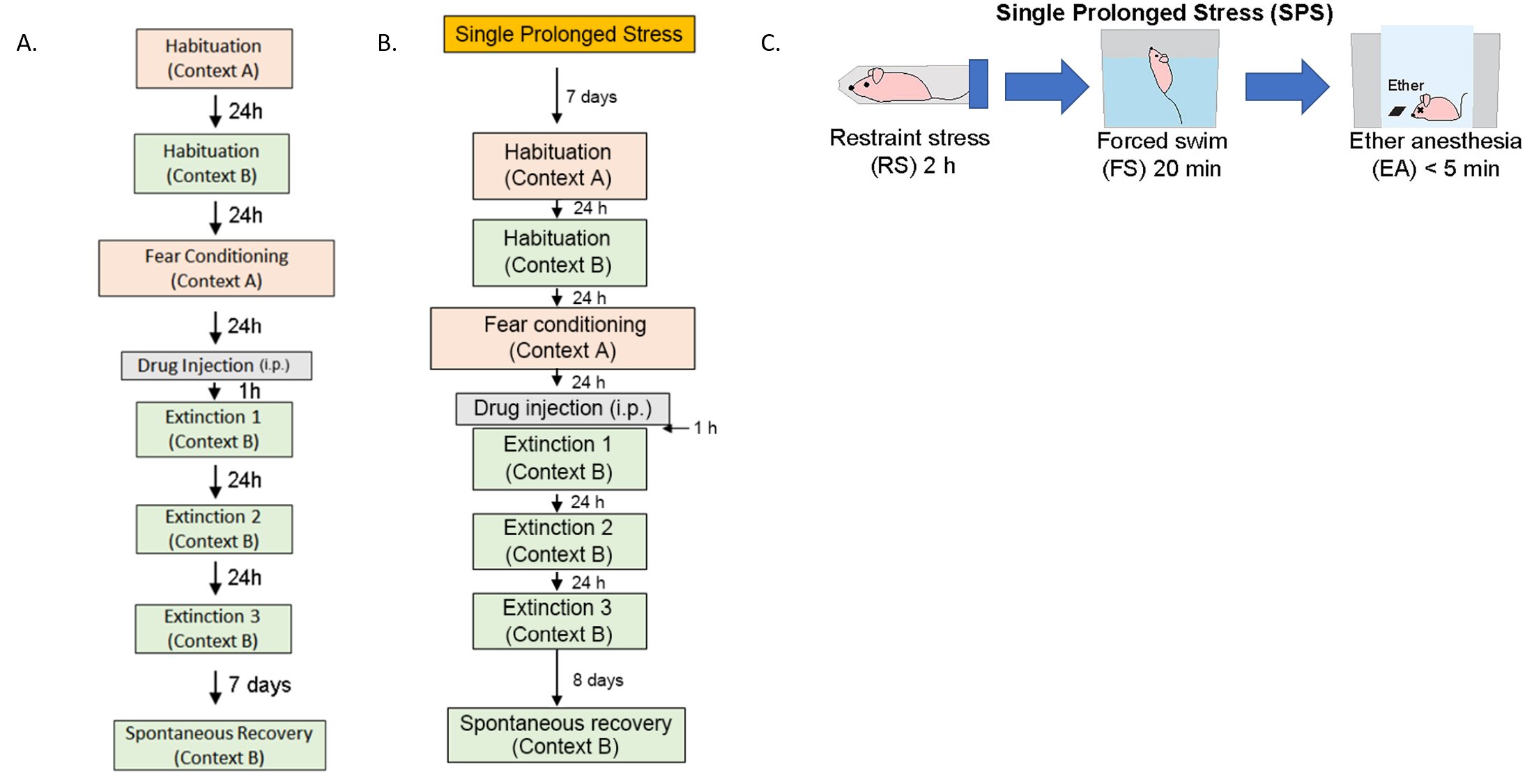
Existem dois modelos de roedores estabelecidos de TEPT: modelos de condicionamento auditivo do medo (AFC) e estresse prolongado único (SPS). Para condicionamento auditivo de medo, os camundongos foram habituados a um ambiente e submetidos a uma combinação de tom e choque elétrico para condicionamento de medo para induzir TEPT. Para induzir um único estresse prolongado, alguns dos camundongos foram expostos a múltiplos estressores para induzir um único estresse prolongado antes do condicionamento do medo. Deve-se notar que a experiência estressante antes do condicionamento do medo é bem conhecida por causar mais dificuldades no tratamento do TEPT posteriormente.
Os camundongos foram então colocados em um novo ambiente e submetidos a uma série de procedimentos de extinção de memória na tentativa de remover suas memórias traumáticas. Para aumentar a terapia cognitivo-comportamental, os pesquisadores testaram o desempenho do NYX-783 junto com a cetamina, que é um conhecido medicamento antidepressivo de ação rápida. Descobriu-se que injetar a droga nos camundongos uma hora antes da terapia de extinção do medo resultou na maior taxa de sucesso do tratamento.
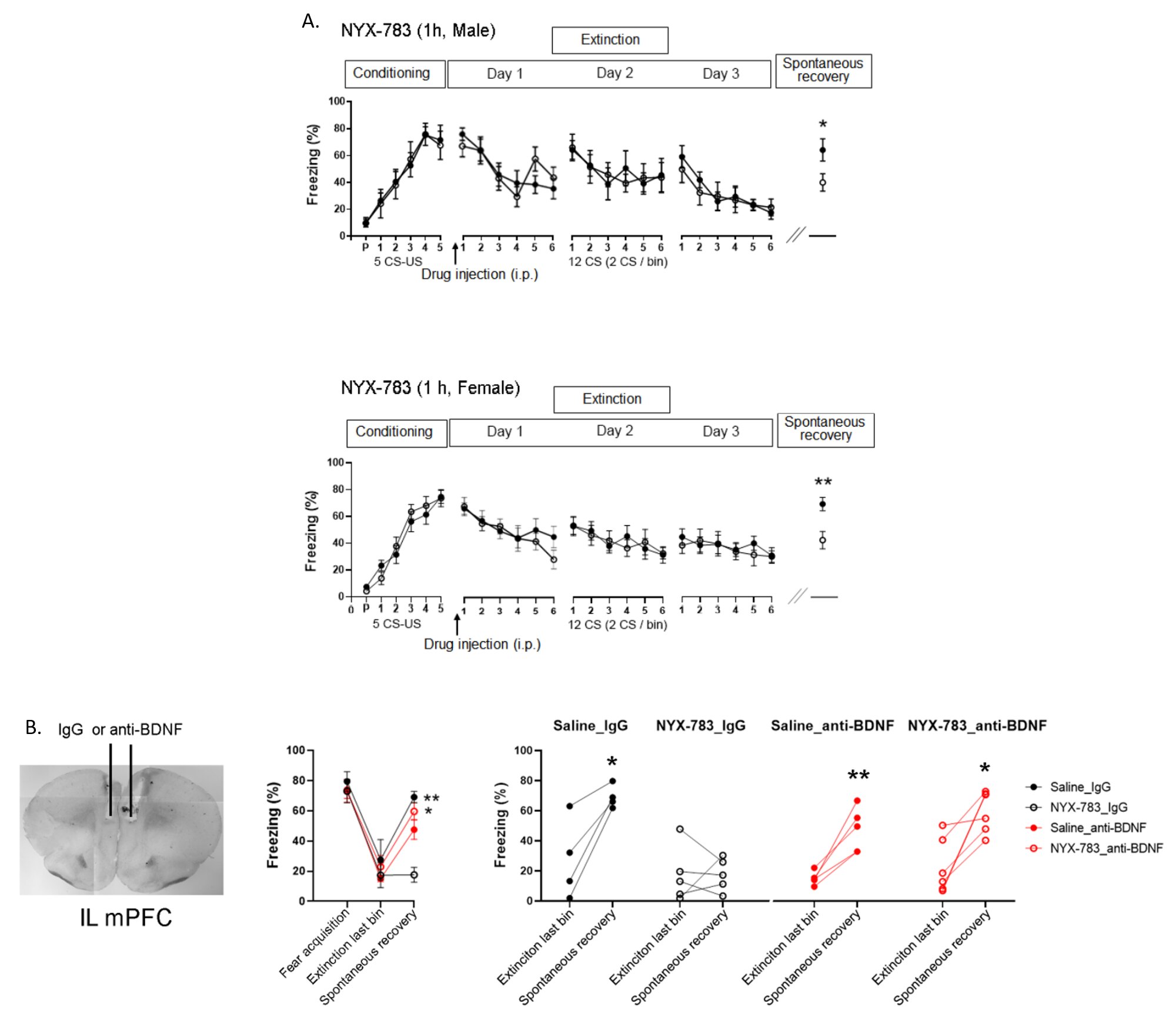
Após o tratamento, os camundongos foram monitorados quanto ao comportamento de congelamento ao ouvir o mesmo som, a fim de medir o nível de medo que estão experimentando. Foi confirmado que os camundongos injetados com NYX-783 se saíram muito melhor do que aqueles injetados com cetamina ou controles salinos. A droga foi particularmente eficaz em suprimir a recuperação espontânea ou o retorno indesejado do TEPT. A droga se comportou de forma diferente dependendo do sexo dos camundongos, com camundongos fêmeas respondendo mais positivamente ao tratamento do que camundongos machos.
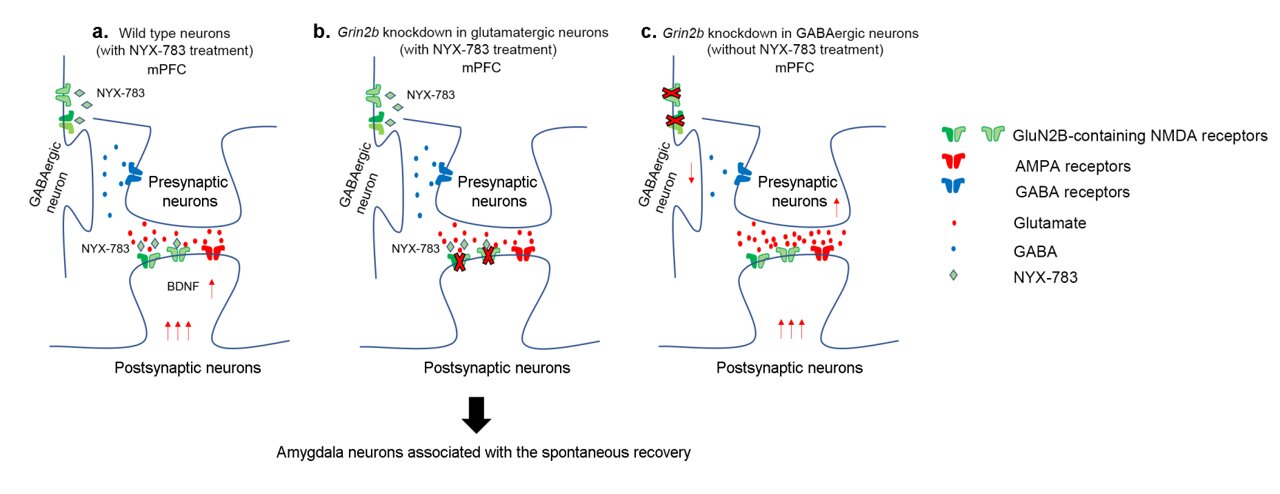
Para explorar o mecanismo do tratamento, esses experimentos foram repetidos em conjunto com a manipulação genética. Primeiro, descobriu-se que o NYX-783 inibe as memórias de medo e suprime a recuperação espontânea dessas memórias modulando os receptores NMDA, especificamente agindo na subunidade GluN2B. Para testar isso, os pesquisadores derrubaram a subunidade GluN2B de NMDARs manipulando o gene Grin2b usando vetores virais. Como esperado, a eficácia da droga diminuiu principalmente quando os receptores foram derrubados em neurônios glutamatérgicos no córtex pré-frontal medial. Em particular, o mutante knockdown Grin2b exibiu recuperação espontânea, mesmo que tenha sido injetado com NYX-783.
Por outro lado, o desempenho da droga não foi afetado quando os mesmos receptores foram derrubados em interneurônios GABAérgicos. Curiosamente, descobriu-se que derrubar os receptores NMDA nos interneurônios sozinho era capaz de reduzir a recuperação espontânea. O grupo acredita que isso é mais provável através da redução dos efeitos inibitórios do interneurônio no neurônio principal.
No entanto, isso não exclui totalmente a possibilidade de NYX-783 atuar nos interneurônios inibitórios. Os autores observaram que “o knockdown do Grin2b em interneurônios sem NYX-783 já mostra baixo congelamento durante a recuperação espontânea. GluN2B em neurônios glutamatérgicos.” Embora se acredite que a atividade da droga no neurônio glutamatérgico seja mais importante para a saída comportamental, mais pesquisas podem ser necessárias para confirmar isso.
Por fim, a equipe descobriu que o fator neurotrófico derivado do cérebro (BDNF), que é altamente importante para a plasticidade sináptica, é necessário para a extinção da memória. Quando os autores suprimiram a atividade do BDNF em cérebros de camundongos usando o tratamento com anticorpos, isso embotou a maior parte do efeito do NYX-783 na inibição da recuperação espontânea.
O autor correspondente Lee Boyoung, do Center for Cognition and Sociality, comentou: “Juntos, esses resultados sugerem que o NYX-783, um novo modulador positivo de NMDAR, pode ser um medicamento eficaz para o TEPT. Embora os estudos clínicos desse composto estejam em andamento, esses resultados sugerem que o desenvolvimento de moduladores NMDAR pode ser uma estratégia viável para tratar PTSD.”
Publicado em 18/04/2022 05h32
Artigo original:
Estudo original:


