COVID-19 forneceu uma oportunidade de mostrar que as vacinas de mRNA podem funcionar. Agora, as empresas farmacêuticas estão correndo para aplicar a plataforma de tecnologia para a gripe.
Após a implantação bem-sucedida de vacinas de mRNA para a prevenção de COVID-19, três farmacêuticos líderes mudaram as vacinas candidatas contra a gripe sazonal construídas com a tecnologia para os primeiros testes clínicos. Mais empresas pretendem seguir sua liderança no próximo ano (Tabela 1).
Esses candidatos, se bem-sucedidos, podem aumentar drasticamente a eficácia de uma classe de vacina que geralmente oferece proteção sem brilho. Para os proponentes do mRNA – liderados por Moderna, Pfizer e Sanofi, todos os quais iniciaram testes de fase I nos últimos meses – novas vacinas contra a gripe podem ser lucrativas ou ajudar a manter a posição em um mercado global projetado para exceder US $ 10 bilhões no final da década.
Selecione vacinas de mRNA para influenza sazonal dentro e abordando a clínica
| Patrocinador |
Nome do produto |
Tecnologia |
Tipo |
Antígeno (s) da gripe |
| Na clínica |
||||
| Moderna |
mRNA-1010 |
mRNA |
Quadrivalente |
Haemagglutinina |
| Sanofi / Translate Bio |
MRT-5400, MRT-5401 |
mRNA a |
Monovalente (H3N2) |
Haemagglutinina |
| Pfizer |
PF-07252220 |
mRNA |
Monovalente (H1N1) e monovalente (B / Yamagata), para ser combinado em bivalente e quadrivalente |
Haemagglutinina |
| Pré-clínico |
||||
| Moderna |
mRNA-1020, mRNA-1030 |
mRNA |
Multivalente |
Hemaglutinina + neuraminidase |
| Moderna |
mRNA-1073 |
mRNA |
Quadrivalente + COVID-19 |
Haemagglutinina |
| Innorna |
mRNA |
Quadrivalente e pentavalente (duas cepas H3N2) |
Haemagglutinina |
|
| Sanofi |
mRNA |
Quadrivalente |
Haemagglutinina |
|
| NIAID |
mRNA |
Monovalente (H1N1) |
Haemagglutinina |
|
| NIAID |
mRNA |
Universal |
Haste de hemaglutinina |
|
| Seqirus |
saRNA |
Quadrivalente |
Haemagglutinina |
|
| Pfizer |
saRNA |
Valência não revelada |
Haemagglutinina |
|
| Arcturus |
Indeciso |
Quadrivalente |
Haemagglutinina |
|
| GSK / CureVac |
Indeciso |
Valência não revelada |
Não divulgado |
aMRT-5400 e MRT-5401 dependem de RNA não modificado. NIAID, Instituto Nacional de Alergia e Doenças Infecciosas; saRNA, RNA de autoamplificação.
Mas as vacinas contra a gripe também podem ser um teste mais desafiador para o mRNA do que o COVID-19. Isso porque, ao contrário do SARS-CoV-2 – para o qual não havia intervenções médicas estabelecidas – nove vacinas contra a gripe de quatro fabricantes diferentes de vacinas já estão disponíveis apenas nos Estados Unidos.
Essas vacinas são seguras, mas sua eficácia deixa espaço para melhorias. As vacinas contra a gripe existentes, sejam construídas em torno de vírus inativados ou proteínas recombinantes, normalmente oferecem apenas 40 a 60% de proteção contra infecções. Em teoria, o mRNA pode ser um produto melhor: as respostas imunes induzidas podem ser mais amplas, as proteínas expressas devem ter melhor fidelidade de sequência, a seleção da cepa pode ser mais precisa e a tecnologia facilita a incorporação de um grande número de antígenos. Todos esses recursos podem se traduzir em maior proteção imunológica.
Mas o mRNA, pelo menos quando formulado em nanopartículas lipídicas (LNPs), está sujeito a problemas de tolerabilidade. Os jabs de mRNA autorizados da Moderna e Pfizer / BioNTech para COVID-19 costumam causar dor nos braços, dores de cabeça, febre baixa e fadiga. Esses mesmos sintomas podem ocorrer com as vacinas contra a gripe aprovadas, mas geralmente são muito mais brandos em grau.
O mRNA “é uma ferramenta que oferece algum potencial positivo”, diz Gary Nabel, ex-CSO da Sanofi, diretor fundador do Vaccine Research Center (VRC) do NIH e CEO da empresa de imunoterapêutica de estágio furtivo ModeX Therapeutics. “O grande obstáculo é a segurança.”
Para impactar o mercado estabelecido, a plataforma precisaria encontrar um ponto ideal mais tolerogênico, além de oferecer grandes vantagens de eficácia.
No entanto, não há certeza de que o mRNA será capaz de fornecer glicoproteínas hemaglutinina, o principal antígeno encontrado nas vacinas contra a gripe. “Tivemos uma sorte incrível com as vacinas COVID por causa do design do antígeno e da imunodominância dessa proteína?” pergunta Anna Blakney, uma bioengenheira de RNA da Universidade de British Columbia. “Ou nós tropeçamos em algo que é funcional para outras glicoproteínas virais também?”
Fazendo isto
Muitos dos principais contendores da gripe baseados em mRNA estavam trabalhando em candidatos à vacina contra a gripe antes da pandemia. Então veio o novo coronavírus, e “nós literalmente trocamos as sequências de codificação da gripe e trocamos as sequências do SARS-CoV-2”, diz Philip Dormitzer, chefe de pesquisa de vacinas virais da Pfizer.
Todo o campo foi beneficiado. Seqirus ficou de fora da corrida da vacina COVID-19, apesar de ter uma plataforma de mRNA de autoamplificação que entrega a sequência de codificação do antígeno e a máquina de replicação necessária para que o construto se copie dentro da célula hospedeira. (A Seqirus adquiriu essa plataforma da Novartis em 2015.) “Ver uma vacina de mRNA funcional e gerar uma resposta tão robusta de certa forma eliminou as preocupações externas que as pessoas podem ter em torno da tecnologia geral”, disse Ethan Settembre, vice-presidente de P&D da Seqirus .
E os benefícios potenciais do mRNA para a profilaxia da gripe são muitos.
Algumas delas se resumem em como as vacinas são feitas. Como as vacinas de mRNA são fabricadas sinteticamente, ao codificar uma sequência de antígeno alvo em um modelo de plasmídeo, elas oferecem alta fidelidade: os antígenos codificados correspondem exatamente às cepas de gripe selecionadas para a vacina de cada ano. Em contraste, as vacinas de vírus inativados que são feitas em sistemas baseados em ovos e células freqüentemente sofrem de mutações de sequência que enfraquecem sua eficácia.
As vacinas de proteína recombinante oferecem a mesma vantagem de fidelidade, mas o processo de fabricação dessas é comparativamente complicado. A flexibilidade e velocidade da produção da vacina de mRNA significam que os fabricantes de vacinas podem esperar mais para começar a fabricação – começando a produção em maio, digamos, em vez de fevereiro, para o hemisfério norte. Isso permitiria que eles tomassem decisões mais informadas sobre quais cepas incluir.
“Cada pouco do tempo ajuda”, diz Sally Mossman, chefe do centro de P&D de vacinas da GlaxoSmithKline nos Estados Unidos.
Entre no multiplex
Pode haver outros benefícios de eficácia. Os EUA contam com vacinas quadrivalentes, contendo antígenos hemaglutinina (purificados de vírus inativados ou fabricados de forma recombinante) ou vírus vivos atenuados que conferem proteção contra quatro cepas de influenza. (Outras jurisdições ainda usam vacinas trivalentes.) Alguns pesquisadores argumentaram a favor da adição de proteção contra cepas adicionais, mas fazer isso é logisticamente desafiador com as plataformas existentes.
Não necessariamente com o mRNA.
Uma equipe liderada por Norbert Pardi, da Escola de Medicina Perelman da Universidade da Pensilvânia, e Raffael Nachbagauer, então na Escola de Medicina Icahn no Monte Sinai, mostrou isso no ano passado. Eles imunizaram camundongos contra um subtipo de gripe com uma vacina de mRNA que codifica quatro proteínas diferentes: haste de hemaglutinina, neuraminidase, canal iônico matriz-2 e nucleoproteína. Junto com Meagan McMahon do Mount Sinai, Pardi e seus colegas repetiram o exercício para dois outros subtipos de gripe. Eles planejam testar uma vacina combinada contendo de 10 a 12 antígenos em camundongos e furões. Idealmente, isso irá induzir uma proteção imunológica tão ampla que não precisa ser tomada todos os anos.
Muitos pesquisadores também esperam que o mRNA estimule respostas imunológicas mais fortes ou mais diversificadas do que as plataformas tradicionais. Se for verdade, isso pode ser especialmente benéfico para adultos mais velhos, que muitas vezes têm respostas fracas às vacinas contra a gripe, observa Jenna Bartley, que estuda o envelhecimento imunológico na Escola de Medicina da Universidade de Connecticut.
Pode até ajudar no desenvolvimento de uma vacina universal contra a gripe que protege contra todas as cepas do vírus, diz Tony Moody da Duke University. Com o apoio do NIH, ele agora está desenvolvendo uma vacina de haste estabilizada com hemaglutinina baseada em mRNA, modelada a partir de uma vacina baseada em proteína que já está na clínica. “É um experimento informativo”, diz o diretor do VRC, John Mascola. “Não sabemos como induzir um alto nível de anticorpos duráveis para o tronco, e o mRNA pode ser diferente na forma como induz essa resposta.”
As tecnologias atuais de vacinas, em sua maioria, provocam apenas respostas humorais que bloqueiam a invasão viral. As vacinas de mRNA, porque de certa forma mimetizam as infecções naturais, podem produzir melhores respostas das células T.
Barney Graham também vê uma oportunidade social mais ampla: ao trabalhar em candidatos sazonais de mRNA hoje, as empresas devem estar mais bem preparadas para enfrentar as pandemias de gripe no futuro. “Esse é o lugar onde o mRNA poderia realmente mudar o negócio”, diz Graham, que se aposentou como vice-diretor do VRC no final de agosto. “Se realmente tivéssemos uma pandemia, você poderia projetar [uma nova vacina] dentro de 10 minutos após receber a sequência, e você poderia ter o mRNA entrando em ação dentro de algumas semanas”.
Mostre-me os dados
Os únicos dados humanos relatados até agora sobre uma vacina contra a gripe baseada em mRNA vêm da primeira investida de Moderna na clínica. No início de 2015, a empresa avaliou um par de vacinas de duas doses, cada uma projetada contra uma cepa diferente da gripe aviária.
De acordo com o ex-CMO Tal Zaks da Moderna, o objetivo principal desses testes era fazer um teste com o mRNA da empresa. “Se você quer mostrar que a tecnologia funciona, o lugar mais fácil para começar é com uma vacina contra a gripe”, diz ele. Com a gripe, explica ele, os correlatos de proteção – medidas de parâmetros imunológicos que permitem predizer a eficácia da vacina – estão bem definidos. Também existem vacinas estabelecidas para referenciar os resultados clínicos.
Para muitos espectadores, os primeiros testes de Moderna foram uma decepção. Embora a maioria dos participantes do estudo que receberam doses mais altas das vacinas experimentais desenvolveram títulos de anticorpos específicos para influenza acima do limite considerado protetor – conforme medido pelo ensaio de inibição da hemaglutinação (HAI) bem validado – esses níveis de anticorpos diminuíram em poucos meses após a imunização . Isso sugere que a proteção que eles oferecem pode ter vida curta. A imunidade das células T não foi detectada de todo.
Ex-executivos da empresa envolvidos nos testes vêem as coisas de maneira diferente. Tanto Giuseppe Ciaramella, ex-chefe de pesquisa de doenças infecciosas, quanto Michael Watson, ex-presidente da unidade de vacinas da Moderna, argumentam que as vacinas induziram um conjunto robusto de células B de memória, que lembram antígenos e podem desencadear a produção rápida de anticorpos quando as pessoas estão curadas. -exposta ao vírus.
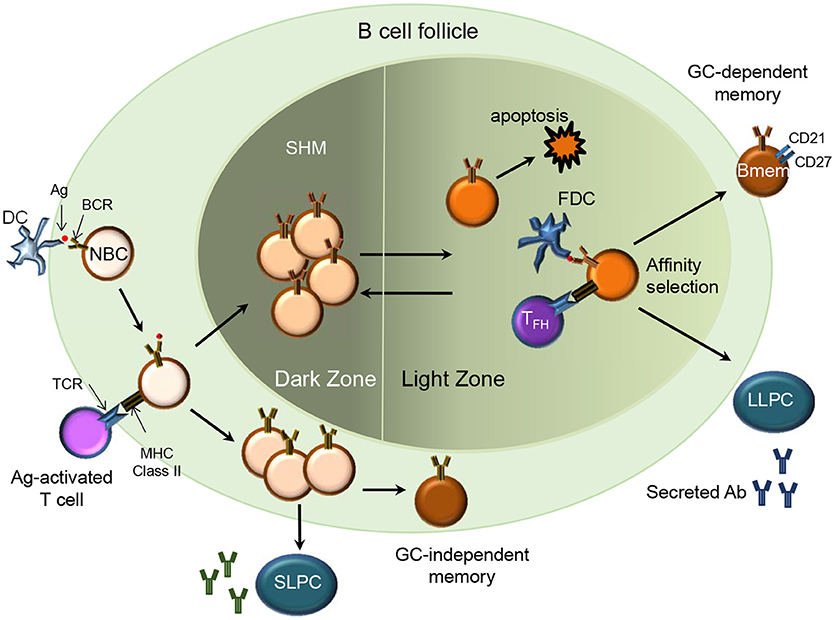
Eles destacam dados de 5 participantes que receberam suas duas injeções com 6 meses de intervalo, em vez de 3 semanas de intervalo, como todo mundo. Esses indivíduos alcançaram títulos médios de HAI muito mais altos – “evidência”, diz Watson, “de que a primeira dose foi preparada muito bem”. Watson é agora presidente executivo da VaxEquity e presidente-executivo da MEVOX, nenhum dos quais está trabalhando com a gripe.
Watson está menos otimista sobre as descobertas de tolerabilidade, no entanto. Embora Moderna tenha mudado sua formulação LNP e aspectos de seu projeto de mRNA, seus dados de testes iniciais sugeriram que o índice terapêutico para uma vacina contra a gripe baseada em mRNA pode ser estreito. Isso pode ser problemático para vacinas contra a gripe sazonal de múltiplos componentes projetadas para treinar o sistema imunológico a reconhecer pelo menos quatro antígenos.
No entanto, a Moderna está progredindo clinicamente – e já começou a adicionar antígenos adicionais à sua próxima geração de produtos contra a gripe. A neuraminidase, outra glicoproteína de superfície, será incluída nos candidatos clínicos subsequentes da empresa. Outros antígenos que podem estimular melhor a imunidade das células T também estão sendo considerados. Além disso, a empresa está preparando vacinas candidatas combinadas que podem proteger contra vários vírus respiratórios. Um deles, para COVID-19 e gripe, deve entrar em testes clínicos no próximo ano.
Mas a adição de alvos antigênicos provavelmente exigirá doses totais de vacina mais altas, aponta Watson, potencialmente desencadeando reações adversas mais graves. “Isso é definitivamente o yin e o yang lá”, diz ele.
Temporada aberta
Nachbagauer, que ingressou na Moderna no ano passado para liderar os esforços de P&D em doenças infecciosas, está ciente das preocupações com a tolerabilidade, mas está adotando uma abordagem de esperar para ver o problema. O primeiro candidato a vacina contra a gripe sazonal da empresa, mRNA-1010, consiste em quatro sequências de mRNA que codificam glicoproteínas hemaglutininas de linhagens virais recomendadas pelas autoridades de saúde globais, formuladas nos mesmos LNPs usados para fornecer a vacina COVID-19 da empresa. “Estamos realmente interessados em como é nossa reatogenicidade”, diz ele.
Os contextos imunológicos em torno das vacinas contra a pandemia e a gripe sazonal são bastante diferentes, acrescenta Nachbagauer. As vacinas contra a pandemia de gripe devem proteger contra uma nova ameaça. Como as pessoas geralmente não têm imunidade preexistente contra eles, um regime de imunização de duas doses e reforço é fundamental. Com a gripe sazonal, a maioria das pessoas foi exposta às cepas relacionadas ou recebeu injeções de gripe anteriores. Portanto, apenas um tiro pode ser suficiente para proteger contra a adaptação mais recente de um adversário em mutação contínua. Se as vacinas COVID-19 servirem de guia, um candidato a uma dose pode ser mais tolerável do que um produto de duas doses.
A Moderna lançou um ensaio de 180 pessoas com dosagem de mRNA-1010 em julho. Espera-se que seja executado até o início de 2022.
A Sanofi e a Pfizer também mudaram suas primeiras vacinas contra a gripe baseadas em mRNA para os testes de fase I. Essas empresas estão adotando abordagens medidas para eliminar o risco de plataformas de mRNA, começando com candidatos contendo apenas um único mRNA que codifica o domínio da cabeça de hemaglutinação de um tipo de vírus da gripe.
A Sanofi está avaliando sua vacina candidata monovalente H3N2 em duas formulações diferentes de LNP. “Se os resultados forem positivos, o desenvolvimento clínico de uma vacina quadrivalente contra a gripe seria o próximo passo”, disse Frank DeRosa, diretor de tecnologia da subsidiária da Sanofi Translate Bio. (A Sanofi adquiriu a Translate no início deste ano por US $ 3,2 bilhões.)
A vacina contra a gripe da empresa, por enquanto, usa uma forma de mRNA que não possui as modificações químicas encontradas na maioria dos outros produtos de mRNA. A vacina COVID-19 da Sanofi, construída em torno desta plataforma de mRNA não modificada, eliciou com sucesso respostas de anticorpos em testes clínicos iniciais. Mas ainda não foi comprovado em um teste de eficácia. A vacina de mRNA COVID-19 não modificada de CureVac tropeçou em ensaios de fase III, no entanto, levantando a possibilidade de que essa estratégia pode ser inferior aos candidatos a mRNA modificado.
Isso talvez explique porque a Sanofi está planejando também ter uma vacina quadrivalente contra a gripe, baseada em mRNA modificado, na clínica no próximo ano. CureVac, em parceria com a GlaxoSmithKline, está considerando as duas opções de mRNA para sua vacina contra a gripe.
Enquanto isso, a Pfizer está avançando com dois programas paralelos: um envolvendo mRNA modificado e outro com uma construção autoamplificadora. Seu candidato a mRNA modificado, PF-07252220, é o primeiro. (A Pfizer licenciou a tecnologia da BioNTech e optou por avançar seu programa de gripe sozinho.) Em setembro, ela começou um ensaio de fase I desta vacina monovalente em quatro níveis de dose, cada injeção contendo um único antígeno de uma gripe tipo A ou B cepa. Ela planeja combiná-los posteriormente em uma vacina bivalente, administrada em diferentes dosagens, antes de passar para um produto quadrivalente – todos comparados com uma vacina contra gripe aprovada.
A Pfizer planeja iniciar testes de seu candidato a mRNA de autoamplificação nos próximos meses.
Um caminho bem trilhado
Para qualquer vacina baseada em mRNA que avança para o teste de estágio posterior, o caminho regulatório para aprovação é bem definido: as empresas precisarão demonstrar eficácia por meio de ensaios clínicos clássicos ou mostrar não inferioridade contra um comparador licenciado em uma medida substituta de proteção, como título HAI. “Essa é a beleza da gripe”, diz Pad Chivukula, diretor científico e diretor de operações da Arcturus Therapeutics. “O caminho para o licenciamento é bastante simples.”
A abordagem de correlação é de menor custo e envolve menos risco, especialmente para vacinas otimizadas para induzir a produção de anticorpos. Mas não vai capturar a proteção acumulada por meio da indução de respostas de células T ou outros braços do sistema imunológico, uma queda potencial para os contendores de mRNA. A abordagem correlata também não oferece suporte a alegações sobre a superioridade da plataforma no que diz respeito à amplitude ou longevidade da proteção. Portanto, a maioria das empresas com vacinas baseadas em mRNA em andamento antecipa eventualmente a realização de testes em grande escala ao longo de uma ou mais temporadas de gripe.
“No final das contas”, diz Dormitzer, “acho que para as pessoas realmente serem convencidas a mudar para uma nova plataforma de vacina, elas vão querer ver a eficácia, bem como todas as comparações imunológicas”.
Embora no ano passado tenha havido uma queda acentuada nos casos de gripe em todo o mundo, provavelmente o resultado do uso de máscaras e do distanciamento social em resposta ao COVID-19, a maioria dos especialistas espera que a gripe volte com violência. Quando isso acontecer, as empresas esperam que suas vacinas candidatas baseadas em mRNA estejam prontas.
Publicado em 14/10/2021 12h38
Artigo original:
Estudo original:


